
Homocisteina
Acest articol este dedicat cresterii patologice a nivelului seric de homocisteina (hiperhomocisteinemia), punctand si caile metabolice de reglare a concentratiei serice, tinand cont in special de mutatiile genetice ale genelor MTHFR, CBS si BHMT, de riscurile clinice si de abordarea terapeutica din perspectiva nutrigenomica.
Diagnostic de laborator
Intervalul de referinta
Intervalul de normalitate pentru homocisteina serica pentru majoritatea laboratoarelor prezentat pe buletinele de rezultate medicale in general este mai mic de 10-12 µmol/L (1).
In functie de varsta si sex, intervalul de normalitate este aproximativ (2):
- varsta 0-30 ani: 4.6-8.1 µmol/L
-
varsta 30-59 ani: 6.3-11.2 µmol/L (sex masculin)
-
varsta 30-59 ani: 4-5-7.9 µmol/L (sex feminin)
-
varsta >59 years: 5.8-11.9 µmol/L
Intervalul optim pentru homocisteina este 6 – 7 µmol/L, desi sunt unii medici care prefera un interval putin mai larg de 5.5 – 7 µmol/L (3).
Intervalele de risc
Clasificarea nivelului homocisteinei serice in functie de gravitate include, (desi aceste valori personal le consider foarte mari, in lumina studiilor clinice care asociaza valori peste 11 µmol/L cu fenomene vasculare) (1):
- Nivel moderat de risc 15-30 µmol/L
- Nivel intermediar de risc 30-100 µmol/L
- Nivel sever de risc >100 µmol/L.
Cauze ale cresterii nivelului de homocisteina serica
Homocisteina este pozitionata metabolic la intersectia a trei cicluri importante, respectiv ciclul folatului, ciclul transsulfurarii si ciclul metilarii, putand astfel sa fie directionata inspre trei cai metabolice, in functie de necesitati (4). Cresteri ale nivelului de homocisteina serica apar in mutatiile genelor enzimelor din cele trei cicluri metabolice, precum si in interferente chimice:
- A. Mutatii care afecteaza reciclarea homocisteinei in metionina prin MTR/MTRR/MTHFR
- B. Mutatii care afecteaza reciclarea homocisteinei in metionina prin BHMT
- C. Mutatii care afecteaza degradarea homocisteinei prin CBS (calea transsulfurarii)
- D. Cresteri ale concentratiei de homocisteina prin interferente medicamentoase.
A. Mutatii care afecteaza reciclarea homocisteinei in metionina prin MTR/MTRR/MTHFR
Conversia homocisteinei (the bad guy) in metionina (the good guy) are loc in ciclul metilarii prin cele doua cai: calea lunga a ciclului metilarii (cu enzimele MTR/MTRR) si cea scurta (cu enzima BHMT).
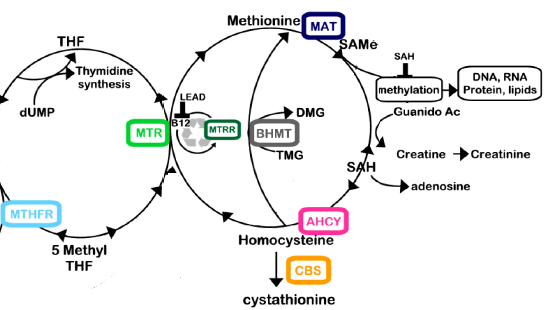 Foto – Cele 3 cicluri ale homocisteinei (5)
Foto – Cele 3 cicluri ale homocisteinei (5)
Calea lunga a ciclului metilarii foloseste urmatoarele enzime si cofactori:
- enzima MTR (Metionin Sintaza) (6)
- enzima MTRR ( Metionin Sintaza Reductaza) cu rol in mentinerea activa a enzimei MTR(7)
- metilcobalamina (vitamina metilB12)
- metilfolat (5 metil-THF) sintetizat de enzima MTHFR in ciclul folatului.
Produsii acestei reactii sunt:
- Metionina (care sustine in ciclul metilarii mai departe sinteza de SAM, adenozina, creatina)
- THF (care este recirculat in ciclul folatului, participa la sinteza de purine si de metilfolat ).
Aceasta este calea principala de metabolizare a homocisteinei, unde daca factorii enumerati prezinta modificari functionale efectul va fi acumularea de homocisteina si cresterea nivelului seric peste limita normala (hiperhomocisteinemia).
Disfunctionalitatea acestei cai metabolice poate apare in prezenta de mutatii ale oricarei gene/enzime implicate:
A1. Prezenta mutatiei MTHFR C677T
Enzima MTHFR catalizeaza reactia de conversie a 5.10 metilen THF in 5 metil THF (metilfolat) necesitand prezenta vitaminei B2 si NAD drept cofactori obligatorii.
Cea mai cunoscuta este mutatia MTHFR C677T (unde mutatia homozigota 677 +/+ este mai grava decat cea heterozigota +/-), care duce la scaderea concentratiei serice de metilfolat si acumulare de homocisteina prin deficit de cofactor.
In aceasta situatie, pentru a face bypass si a compensa defectul genetic/metabolic se suplimenteaza direct cu metilfolat .
Suplimentarea cu acid folic este contraindicata, deoarece acesta:
- inhiba suplimentar enzima MTHFR, care este oricum deficienta functional datorita mutatiei 677 (8)
- trebuie transformat in mai multe etape enzimatice in metilfolat , ultima etapa fiind cea catalizata de MTHFR, care are o eficienta redusa la 60% pentru varianta heterozigota si 30% pentru homozigota.

Foto – Mutatia MTHFR 677 (9)
A2. Prezenta de mutatii ale genei MTR
Enzima MTR sau Metionin Sintaza necesita drept cofactori vitamina B12 reciclata (metilcobalamina) si Zinc (Zn2+) pentru a cataliza reactia de conversie a homocisteinei in metionina. Dupa cum se poate vedea in imaginea proteinei MTR de mai jos, zincul este localizat in centrul activ enzimatic.
Deficitul de vitamina B12 va avea acelasi efect ca si mutatia genei MTR, cresterea homocisteinemiei serice.
Mutatiile MTR de tip MTR A2756G au ca efect up-regularea enzimei MTR, cu consum rapid de metilfolat si metil-B12 si consecutiv, paradoxal, acumulare de homocisteina prin deficit de cofactori.
Pentru a sustine conversia excesului de homocisteina in metionina in aceasta situatie se suplimenteaza cu :
- metilfolat
- metilB12 sau adenozil B12, in functie de statusul mutatiilor COMT
- NU se suplimenteaza cu cianB12 (ciancobalamina).
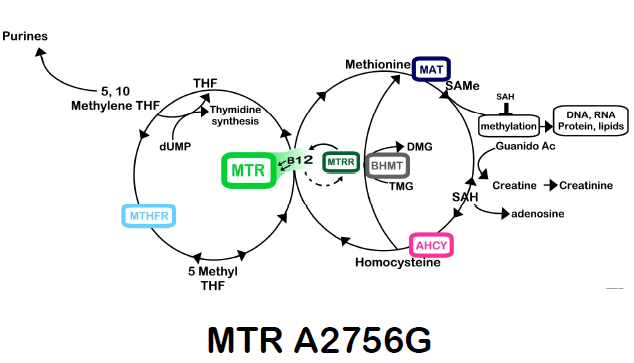
Enzima MTR poate avea o activitate diminuata ceea ce duce la scaderea SAM, cresterea SAH si cresterea homocisteinemiei prin inhibitia data de
- plumb
- acetilaldehida – produs din metabolismul alcoolului sau Candida (10)
- protoxid de azot – inhalosedare
- mercur
Foto – Mutatia MTR (5)
A3. Prezenta de mutatii ale genei MTRR
 Foto -Mutatia MTRR (5)
Foto -Mutatia MTRR (5)
Enzima MTRR (Metionin Sintaza Reductaza) cu rol in mentinerea permanent activa a enzimei MTR.
Enzima MTRR necesita drept cofactor vitamina B2 (riboflavina) pentru a putea cataliza reactia de reciclare a vitaminei B12 (care este cofactor pentru enzima MTR/Metionin Sintaza). Deficienta de vitamina B2 va duce la scaderea activitatii enzimei MTRR.
Mutatiile MTRR de tip MTRR A66G de tip down-regulation vor duce la scaderea performantei enzimei MTRR, cu scaderea metil-B12, scaderea reciclarii metioninei din homocisteina, acumulare de homocisteina si scaderea eficientei ciclului metilarii cu scadere sinteza SAM si afectarea tuturor reactiilor de tip metil-transferaza ce necesita SAM.
Pentru a sustine conversia excesului de homocisteina in metionina in aceasta situatie se suplimenteaza cu metil-B12 sau hidroxi-B12, in functie de toleranta la gruparile metil (status mutatii COMT).
Trebuie sa mentionez ca B12 de tip adenozil nu afecteaza nivelul homocisteinei serice.
B.Mutatii care afecteaza reciclarea homocisteinei in metionina prin BHMT

Aceasta reactie de back-up este folosita in special cand reactia principala de conversie a homocisteinei in metionina nu are loc cu eficienta datorita mutatiilor MTHFR, MTR, MTRR sau prezentei inhibitorilor.
Foto – Mutatia BHMT (5)
Necesita pentru functionare prezenta unei enzime competente BHMT (Betain Homocistein Metil Transferaza) dependenta de zinc.
Reactia pe scurt este: TMG (donor de metil) + Homocisteina (donor de hidrogen) => DMG (receptor de hidrogen) + Metionina (receptor de metil).
Enzima BHMT este prezenta insa numai in ficat si rinichi. (11)
Este stimulata de:
- fosfatidilserina
- fosfatidilcolina
- TMG (tri-metil-glicina)
- restrictia de metionina.
Este inhibata de:
- DMG (di-metil-glicina)
- stres.
Dezavantajele acestei cai metabolice este ca nu se genereaza molecule de SAM, creatina, ADN, ARN, precum in cazul caii metabolice prin MTR/MTRR.
De aceea, pentru a sustine organismul (in timp ce se foloseste aceasta cale pentru a indeparta excesul de homocisteina) se folosesc:
- fosfatidilcolina si TMG – (pentru stimularea BHMT) – atentie insa la statusul COMT, intrucat fosfatidilcolina si TMG sunt donori de grupari metil.
- metilfolat si acid folinic – (care ar fi produse in mod normal daca s-ar folosi calea lunga cu sinteza de THF).
C. Mutatii care afecteaza degradarea homocisteinei prin CBS (calea transsulfurarii)
Homocisteina poate fi degradata in celulele hepatice prin ciclul transsulfurarii, coordonata de enzima CBS (Cistation Beta Sintetaza), o enzima care scoate homocisteina din ciclul metilarii si o transforma in cistation, ce va fi apoi metabolizat in molecule ce contin sulf (taurina, sulfiti, glutation), alfa -ketoglutarat, amoniac.
Cand nivelul de homocisteina creste, organismul reactioneaza prin directionarea crescuta a homocisteinei spre degradare in ciclul transsulfurarii cu sinteza crescuta de glutation principalul antioxidant al organismului), sulfiti si amoniac.
Mutatiile CBS sunt implicate in fenomene vasculare si sunt de tip:
- down-regulation – toate mutatiile
- tip up-regulation – la pacient cu sindrom Down unde exista 3 cromozomi nr. 21, cu expresie crescuta de gena CBS intrucat geba CBS este situata tot pe cromozomul 21.
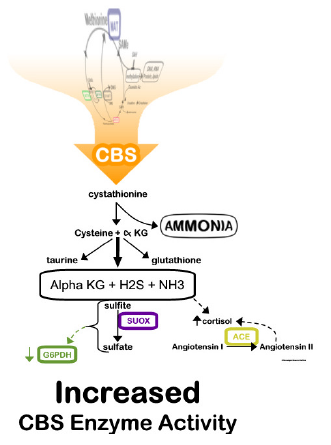
1.Up-regulation (pacient cu sindrom Down)
- pierdere de homocisteina in ciclul transsulfurarii, cu homocisteina serica normala sau scazuta, cu deficienta de homocisteina care intra in ciclul metilarii, cu deficienta procesului de metilare, de sinteza de SAM, ADN, ARN etc
- deficienta de BH4 ce predispune la disfunctie a eNOS (endothelial Nitric Oxid Sintaza) care va converti arginina in radicali liberi (superoxid and peroxinitrit) in loc de oxid
nitric (cu rol ateroprotectiv vasodilator), ce predispun la hipertensiune si o stare inflamatorie cardiovasculara - cei care au suplimentar o functie redusa a enzimelor antioxidante
- SOD (SuperOxid Dismutaza),
- CAT (Catalaza),
- GPX (Glutation PeroXidaza),
- PON1 (ParaOxoNaza) vor avea o provocare metabolica suplimentara in a face fata radicalilor liberi.
- cu exces de amoniac, exces alfa keto glutarat, exces de sulfit de hidrogen
- cu exces de compusi pe baza de sulf si intoleranta la alimente ce contin sulf – glutation, N-Acetil-cisteina.
2. Down-regulation
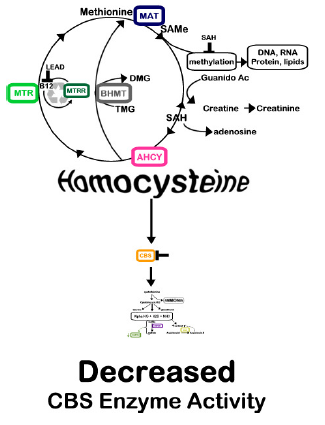
- acumularea de homocisteina in circulatie cu fenomene clinice descrise.
- scaderea sintezei de cistation, glutation.
Foto – Mutatiile CBS cu up si down regulation (5)
D. Interferente medicamentoase
Recomand verificarea prezentei mutatiilor genelor citocromului P450 fata de medicamentele recomandate cu ajutorului tabelului Flockhart.
Medicamente care cresc homocisteina serica (2, 12):
- anti-folatii (metotrexat, 5F-uracil)
- anti-convulsivantele (Levodopa)
- lipid-lowering (Fenofibrat, Bezafibrat)
- anti-inflamatoare nesteroidiene AINS
- Azaribin
- Cafeina
- Cholestiramin
- Colestipol
- Colchicina
- Metformin
- Niacin
- Nitrous oxide
- Pemetrexed
- Fenitoin
- Pirimetamina
- Sulfasalazina
Persoanele care au mutatii ale genelor MTHFR, MTR, MTRR, BHMT, CBS, COMT trebuie sa fie foarte prudente in folosirea medicamentelor din lista de mai sus, pentru a nu potenta cresterea nivelului de homocisteina si a risca un eveniment trombotic.
Desi nu face strict parte din aceasta categorie, aportul prin dieta bogata in proteine animale este de asemenea implicat in cresterea homocisteinei serice.
Implicatiile clinice ale hiperhomocisteinemiei
Riscul de boala vasculara prin ateroscleroza
Homocisteina este un factor de risc independent pentru boala vasculara.
Mecanismele prin care homocisteina promoveaza leziunea vasculara includ:
- stimularea trombozei
- consumul de oxid nitric
- injurie endoteliala (13)
- promovarea inflamatiei prin cresterea expresiei de mocule de adeziune vascualara VCAM1 si TNF alfa
- creste oxidara proteinelor cu densitate mica LDL
- activeaza trombocitele si stimleaza expresia CD40/CD40 ligand
- CD40 stimuleaza eiberarea de interleukine pro-inflamatorii si chemokine CCL2
- creste concentratia de factor tisular procoagulant
- reduce activitatea antitrombinei III (14).
Nivelul crescut de homocisteina din circulatie este un factor de risc pentru boala coronariana fiind in acelasi timp si un factor de prognostic pentru bolnavii cu diagnostic de boala coronariana.
Studiul prospectiv efectuat de Nygård O et al (Department of Public Health and Primary Health Care, University of Bergen, Haukeland University Hospital, Norway) intre 1991-1992 pe 587 de pacienti, cu boala coronariana confirmata angografic, a aratat ca exista o relatie direct proportionala intre nivelul de homocisteina din circulatie si mortalitate (15, 16).
Homocisteinemia (micromol/L) si riscul de deces (95CI%):
- Homocisteina <9.0 este asociata cu risc de deces 1.00 (esantionul baza de comparatie)
- Homocisteina 9.0 – 14.9 este asociata cu risc de deces de 2.35 ori mai mare (0.92-6.03)
- Homocisteina 15.0 – 19.9 este asociata cu risc de deces de 5.75 ori mai mare (2.05-16.01)
- Homocisteina >20.0 este asociata cu risc de deces de 7.04 ori mai mare (2.23-22.4)
Hiperhomocisteinemia si mutatiile COMT
Riscul de a dezvolta o boala cardiovasculara este influentat atat de nivelul de homocisteina serica, precum si de statusul mutatiilor genei COMT (17).
Riscul de a dezvolta o boala vasculara prin hiperhomocisteinemie este potentat de mutatiile suplimentare ale genei COMT. Enzima COMT are efect catalitic in degradarea si inactivarea epinefrinei, norepinefrinei, dopaminei la nivel cerebral si vascular, iar mutatiilor genei COMT vor avea ca efect aparitia simptomelor asociate cu hipertensiunea arteriale, aritmii, tulburari de circulatie periferica.
Hiperhomocisteinemia inhiba direct enzima COMT, prin inhibitia formarii de homocisteina din SAH, astfel SAH se mentine crescut si inhiba COMT.
Daca la o homocisteina marita (care duce la inhibitie chimica a COMT) se adauga si o disfunctie COMT genetica sau dobandita, persoana va avea o functie restanta COMT mult diminuata, cumulul de factori de risc determinand un risc total marit pentru boli cardiovasculare.
Hiperhomocisteinemia este factor de risc pentru tromboza, deficienta activitatii COMT are efecte negative la nivel cardiovascular, iar cand ambele sunt prezente se potenteaza efectul metabolic si se ajunge la un dezechilibru metabolic major.
In studiul prospectiv “Functional COMT Val158Met Polymorphism, Risk of Acute Coronary Events and Serum Homocysteine: The Kuopio Ischaemic Heart Disease Risk Factor Study”, au fost urmariti 792 de barbati finlandezi fara boala cardiaca la care s-a testat prezenta mutatiei COMT V158M, timp de o perioada 9.3 ani, in care 69 dintre ei au dezvoltat sindrom coronarian (18).
Rezultatele studiului arata:
- Risc mic: homocisteina < 11.3 & COMT normala: risc relativ = 1 (baza de comparatie)
- Risc mediu: homocistena > 11.3 & COMT nomala: risc relativ: 1.15 ori mai mare
- Risc inalt: homocisteina < 11.3 & COMT homozigot: risc relativ =1.42 ori mai mare
- Risc foarte inalt: homocisteina > 11.3 & COMT homozigot: risc relativ = 2.6 ori mai mare
Astfel, cunoasterea statusului mutatiilor COMT este necesara atat la persoanele cu homocisteina marita, cat si la cei care au deja antecedente personale patologice de boala cardiaca.
Riscul de accident vascular cerebral
Hiperhomocisteinemia este in acelasi timp si un factor de risc pentru aparitia accidentului vascular cerebral.
Studiul prospectiv efectuat de Iso H et al (Department of Public Health Medicine, Institute of Community Medicine, University of Tsukuba, 1-1-1 Tennodai, Tsukuba-shi, Ibaraki-ken 305-8575, Japan) intre 1984 si 1995 si 1989 si 1995, pe 11.846 de participanti intre 40 si 85 ani a evidentiat urmatoarele riscuri (19):
Homocisteinemia (micromol/L) si riscul TOTAL de accident vascular cerebral (95CI%):
- Homocisteina 4.1 – 7.0 este asociata cu risc de 1.00 (esantionul baza de comparatie)
- Homocisteina 7.0 – 8.7 este asociata cu risc de 1.09 ori mai mare (0.58–2.02)
- Homocisteina 8.7 – 11.1 este asociata cu risc de 1.13 ori mai mare(0.57–2.26)
- Homocisteina >11.1 este asociata cu risc de 2.99 ori mai mare (1.51–5.93)
Homocisteinemia (micromol/L) si riscul de accident vascular cerebral ISCHEMIC (95CI%):
- Homocisteina 4.1 – 7.0 este asociata cu risc de 1.00 (esantionul baza de comparatie)
- Homocisteina 7.0 – 8.7 este asociata cu risc de 1.36 ori mai mare (0.60–3.09)
- Homocisteina 8.7 – 11.1 este asociata cu risc de 1.45 ori mai mare (0.60–3.49)
- Homocisteina >11.1 este asociata cu risc de 3.89 ori mai mare(1.60–9.46)
Homocisteinemia (micromol/L) si riscul de accident vascular cerebral INFARCTE LACUNARE (95CI%):
- Homocisteina 4.1 – 7.0 este asociata cu risc de 1.00 (esantionul baza de comparatie)
- Homocisteina 7.0 – 8.7 este asociata cu risc de 1.19 ori mai mare (0.49–2.88)
- Homocisteina 8.7 – 11.1 este asociata cu risc de 1.04 ori mai mare(0.39–2.80)
- Homocisteina >11.1 este asociata cu risc de 3.36 ori mai mare (1.27–8.90)
Riscul de tromboza in sarcina
Intrucat hiperhomocisteinemia este factor de risc independent de tromboza, se adauga riscului dat de sarcina in sine. In plus, pot exista si alti factori de risc pentru tromboza:
- factori generali: sedentarism, fumat, obezitate, hipercolesterolemie, imobilizare prelungita
- factori ereditari frecventi: trombofiliile ereditare (Factor Leiden, Factor VHR2, Factor II G20210A, MTHFR C677T, PAI-1 4G/5G, Factor XIII Val34Leu, deficienta de ATIII, Proteina C, proteina S)
- factori ereditari rari: anomalii Factor VII, XII, crestere Factor VIII, IX, XI, deficienta cofactor II heparina, de trombomodulin, anomalii plasminogen
- factori dobanditi: diabet zaharat, ateroscleroza, sindroame de hipervascozitate, sindrom antifosfolipidic, administrare de anticonceptionale orale etc.
Nivelul de homocisteina serica trebuie verificat in sarcina mai ales la cele cu mutatii ale genelor implicate in metabolismul homocisteinei: MTHFR, CBS, BHMT, COMT.
S-au observat cresteri ale homocisteinei serice la gravidele cu complicatii incluzand preeclampsia (hipertensiune in sarcina ce poate avea consecinte grave), abruptio placentae (placenta se detaseaza de uter), pierderi repetate de sarcini, restrictie de crestere intrauterina (20).
De asemenea, hiperhomocisteinemia este observata mai frecvent la femeile care au sarcini cu defecte de tub neural (spina bifida, anencefalie), 20% din femeile ce au un copil cu defect de tub neural au defecte in metabolismul homocisteinei (20).
Atitudine terapeutica
Petru o atitudinea terapeutica complexa se trateaza pacientul, nu mutatia sau mutatiile genetice pe care pacientul le prezinta.
Se iau in considerare toate caile metabolice prezentate anterior, pentru aceasta este nevoie de maparea genetica complexa oferita de ancestry.com (sau alt test asemanator), precum si de rezultatele analizelor de laborator.
Dieta si stil de viata
- Se recomanda dieta saraca in metionina / proteine de origine animala pentrua nu supraincarca ciclul metilarii si a creste homocisteina suplimentar
- Se prefera surse de proteina vegetala mai saraca in metionina – fasole, linte si alte leguminoase din fam lor; seminte, nuci, alge marine, ciuperci etc
- Se interzice consumul de alcool deoarece inhiba enzima MTR si creste direct homocisteinemia
- Se interzice consumul de cafea si de medicamente care duc la cresterea homocisteinemiei
- Se folosesc cat mai multe legume verzi crude neprocesate termic – salate, spanac, broccoli, asparag, gulie, castraveti, pentru aport crescut de folat natural
- Se adauga sfecla rosie cruda sub forma de suc proaspat (simplu sau cu morcov/mar/ghimbir) sau salata pentru aport de betaina care stimuleaza calea scurta a conversiei homocisteinei in metionina cu enzima BHMT.
- Se folosesc cat mai multe surse naturale de folat (legume verzi crude, fasole, citrice etc)
- Pentru pacientii cu intoleranta la sulf, se evita alimentele bogate in sulf (ceapa, usturoi, oua, brocoli, varza) si suplimentele ce contin sulf (Glutation, N-Acetil Cisteina, Taurina)
Vitamine si suplimente
Ca linii generale de tratament, pentru compensarea metabolica (bypass) a mutatiilor genetice:
- se administreaza metilfolat (5-MTHF) in cazul mutatiei MTHFR 677, in doze variabile, cu monitorizare permanenta :
- nivelul seric de homocisteina (marker indirect de deficienta)
- concentratia intraeritrocitara si serica de folat (marker direct)
- se administreaza vitamina B12 in cazul mutatiilor MTR:metilcobalamina (metilB12) sau hidroxicobalamina care au efect de scadere a nivelului de homocisteina serica
- NU se foloseste adenozilcobalamina pentru hiperhomocisteinemie intrucat acest tip de B12 nu are efect pe homocisteina serica
- NU se foloseste vitamina B12 de tip ciancobalamina – pentru detalii cititi articolul Ciancobalamina si MTHFR 677: contraindicatii si alternative
- se administreaza metilfolat si metilcobalamina in cazul mutatiilor MTRR unde exista deficit de cofactori
- se administreaza fosfatidilserina si fosfatidilcolina
- pentru stimularea enzimei BHMT, in cazul in care exista mutatii pe calea lunga a ciclului metilarii
- pentru scaderea homocisteinemiei de la valorile periculoase catre un nivel optim
- dieta bogata in vitaminele:B2 si B3 (pentru sustinerea functiei reziduale a enzimei MTHFR)
- B6 (de tip P5P pentru sustinerea enzimei CBS)
- B2, B12 si Zn2+ (pentru sustinerea enzimelor MTR/MTRR)
- interdictie de a lua acid folic, care va actiona competitiv:
- cu metilfolat –ul pentru a actiona la nivel celular pe receptorii celulari
- cu BH2 la nivelul enzimei DHPR la nivel hepatic care are rol de reducere pentru ambele molecule
- se face chelare pentru eliminarea plumbului care are efect inhibitor pe enzima MTR si incetineste eficienta ciclului metilarii
- se suplimenteaza cu un produs complex care contine toti nutrientii si cofactorii necesari pentru functionarea ciclului metilarii (B2, B6, metilfolat, TMG, B12).
- se suplimenteaza cu ulei de peste cu acizi grasi esentiali Omega 3 care stimuleaza functia enzimei MTHFR de a sintetiza metilfolat.
Pentru mai multe detalii legate de Omega 3, am scris articolul MTHFR si Omega 3.
Inainte si la sfarsitul unei cure de tratament cu ulei de peste se recomanda testarea raportului Omega 6:Omega 3 care ideal ar trebui sa fie 1:1.
Suport enzimatic
Aditional, se poate sustine functia enzimelor prin adaos de cofactori, stimularea eliminarii de substante toxice, diverse:
- Suplimentare cu carbune medicinal seara la culcare pentru a scadea incarcarea cu amoniac intestinal produs de flora bacteriana (atentie are ca efect advers constipatie)
- Suplimentare cu magneziu citrat pentru a preveni constipatia data de carbunele medicinal si a sustine functia enzimei COMT intrucat este cofactor
- Se administreaza probiotice de 2-3 ori pe zi pentru a echilibra flora intestinala normala
- Pentru pacientii cu hiperamoniemie, se poate recurge la administrarea de ornitina/aspartat/citrulina pentru stimularea ciclului ureei si scaderea concentratiei de amoniac.
- Pentru mutatiile cu scaderea concentratiei de BH4 se poate administra supliment de BH4
- Suplimentare direct cu forma activa a vitamine B6 de tip P5P
- Suplimentare cu antioxidanti de ex. vitamina C.
Managementul stresului
- Exercitiu fizic moderat
- Somn minim 8-9 ore.
- Evitarea stresului care aduce un plus suplimentar de hormoni de stres.
- Tehnici de relaxare: muzicoterapie, etc.
Referinte
- http://www.emedicinehealth.com/homocysteine/page4_em.htm
- http://emedicine.medscape.com/article/2085682-overview
- http://drfairchild.blogspot.ro/2013/10/mthfr.html
- http://www.beyondmthfr.com/mthfr-and-homocysteine-part-i/
- sursa foto https://www.knowyourgenetics.com/media/pdf/Genetic%20Bypass.pdf
- https://ghr.nlm.nih.gov/gene/MTR
- https://ghr.nlm.nih.gov/ge/MTRR
- http://ajcn.nutrition.org/content/early/2015/01/07/ajcn.114.086603
- http://www.heartfixer.com/AMRI-Outcomes-Non-CV-Autism-Methyl%20Cycle.htm
- https://pubs.niaaa.nih.gov/publications/arcr351/25-35.htm
- https://www.ncbi.nlm.nih.gov/pubmed/9281325
- http://www.lifeextension.com/Magazine/2009/8/Is-Homocysteine-Making-You-Sick/Page-02
- https://www.ncbi.nlm.nih.gov/pubmed/14728038
- http://www.mayoclinicproceedings.org/article/S0025-6196(11)60636-8/fulltext?mobileUi=0
- https://www.ncbi.nlm.nih.gov/pubmed/9227928
- http://www.lifeextension.com/magazine/2006/6/report_doctors/page-01
- http://www.heartfixer.com/AMRI-Nutrigenomics.htm#COMT: Catechol–O–Methyl Transferase and VDR: Vitamin D Receptor
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1779620/
- http://circ.ahajournals.org/content/109/22/2766
- http://circ.ahajournals.org/content/111/19/e289#ref-7
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3612440/
- https://www.ncbi.nlm.nih.gov/pubmed/26211735
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3588400/
Solicitare de Consiliere nutritionala personalizata

Pentru a va programa la o consultatie nutritionala online cu primirea unui tratament nutritional personalizat, puteti lua legatura cu mine prin:
- pagina de Contact.
- e-mail la office@nutrigenomic.ro
- formularul de mai jos.
(14) Comments